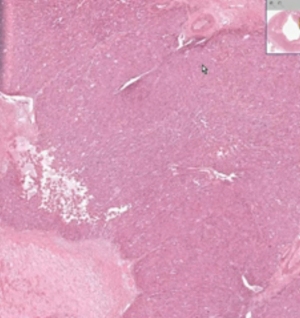
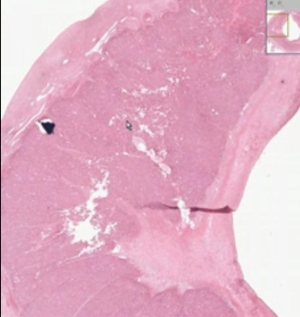
Tumor Wilms
Tumor Wilms
Wilms’ tumor atau nephroblastoma adalah tumor pada ginjal yang biasanya terjadi pada anak-anak, jarang pada orang dewasa. [1] yang merupakan nama umum eponym, merujuk ke Dr Max Wilms, ahli bedah di Jerman (1867-1918) yang pertama ini dijelaskan jenis tumor. [2]
Approximately 500 cases are diagnosed in the US annually. Kira-kira 500 kasus yang didiagnosis di AS per tahun. The majority (75%) occur in otherwise normal children; a minority (25%) is associated with other developmental abnormalities. Sebagian besar (75%) terjadi pada anak-anak normal lain; minoritas (25%) adalah terkait dengan pembangunan lainnya abnormalities. It is highly responsive to treatment, with about 90% of patients surviving at least five years. Sangat responsif terhadap pengobatan, dengan sekitar 90% dari pasien hidup setidaknya lima tahun.
BATASAN
Tumor Wilms adalah tumor ganas embrional ginjal yang berasal dari metanefros. Nama lain tumor ini adalah nefroblastoma atau embrioma renal.
EPIDEMIOLOGI
Tumor wilms merupakan tumor ganas ginjal yang terbanyak pada bayi dan anak. Sekitar 80% tumor ini terjadi pada anak di bawah 6 tahun, dengan puncak insidens pada umur 2-4 tahun. Tumor Wilms dapat juga dijumpai pada neonatus. Tumor Wilms terhitung 6% dari seluruh penyakit keganasan pada anak.
Insiden penyakit ini hampir sama di setiap negara, karena tidak ada perbedaan ras, iklim dan lingkungan, yaitu diperkirakan 8 per 1 juta anak di bawah umur 15 tahun. Perbandingan insiden laki-laki dan perempuan hampir sama. Lokasi tumor biasanya unilateral, lebih sering di sebelah kiri, bisa juga bilateral (sekitar 5%).
ETIOLOGI
Tumor Wilms berasal dari proliferasi patologik blastema metanefron akibat tidak adanya stimulasi yang normal dari duktus metanefron untuk menghasilkan tubuli dan glomeruli yang berdiferensiasi baik. Perkembangan blastema renalis untuk membentuk struktur ginjal terjadi pada umur kehamilan 8-34 minggu. Sehinga diperkirakan bahwa kemampuan blastema primitif untuk merintis jalan ke arah pembentukan tumor Wilms, apakah sebagai mutasi germinal atau somatik, itu terjadi pada usia kehamilan 8-34 minggu.
Sekitar 1,5% penderita mempunyai saudara atau anggota keluarga lain yang juga menderita tumor Wilms. Hampir semua kasus unilateral tidak bersifat keturunan yang berbeda dengan kasus tumor bilateral. Sekitar 7-10% kasus Tumor Wilms diturunkan secara autosomal dominan. Mekanisme genetik yang berkaitan dengan penyakit ini, belum sepenuhnya diketahui. Pada penderita sindrom WAGR (tumor Wilms, aniridia, malformasi genital dan retadasi mental) memperlihatkan adanya delesi sitogenetik pada kromosom 11, daerah p13. Pada beberapa penderita, ditemukan gen WT1 pada lengan pendek kromosom 11, daerah p13. Gen WT1 secara spesifik berekspresi di ginjal dan dikenal sebagai faktor transkripsi yang diduga bertanggung jawab untuk berkembangnya
tumor Wilms.
PATOLOGI
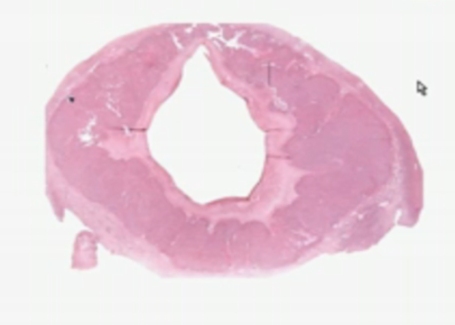
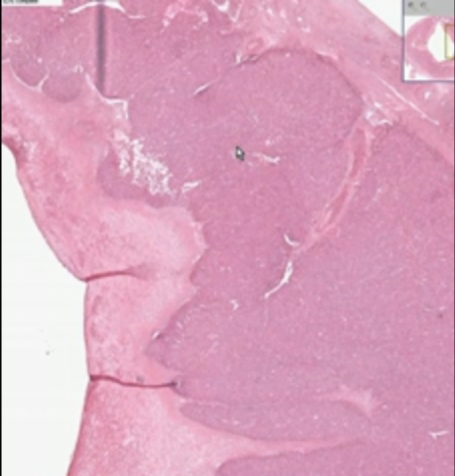
Tumor Wilms tersusun dari jaringan blastema metanefrik primitif. Disamping itu tumor ini sering mengandung jaringan yang tidak biasanya terdapat pada metanefron normal, misalnya jaringan tulang, tulang rawan dan epitel skuamous. Gambaran histologik yang sangat beragam merupakan suatu ciri dari tumor Wilms. Gambaran klasik tumor Wilms bersifat trifasik, termasuk sel epitel blastema dan stroma. Berdasarkan korelasi histologis dan klinis, gambaran histopatologik tumor Wilms dapat dikelompokkan dalam tiga kelompok, yaitu tumor risiko rendah (favourable), tumor risiko sedang dan tumor risiko tinggi (unfavourable).
Stadium
The National Wilms Tumor Study (NWTS) membagi 5 stadium tumor Wilms, yaitu :
Stadium I
Tumor terbatas di dalam jaringan ginjal tanpa menembus kapsul. Tumor ini dapat di reseksi dengan lengkap.
Stadium II
Tumor menembus kapsul dan meluas masuk ke dalam jaringan ginjal dan sekitar ginjal yaitu jaringan perirenal, hilus renalis, vena renalis dan kelenjar limfe para-aortal. Tumor masih dapat direseksi dengan lengkap.
Stadium III
Tumor menyebar ke rongga abdomen (perkontinuitatum), misalnya ke hepar, peritoneum dan lain-lain.
Stadium IV
Tumor menyebar secara hematogen ke rongga abdomen, paru-paru,otak dan tulang.
Sebelum diberikan kemoterapi, ada beberapa evaluasi yang harus dilakukan :
- Anamnesa : apakah ada keluarga yang menderita willms tumor, penyakit yang menyertai, riwayat keluarga untuk kanker, kelainan
kongenital, tumor jinak. - Diagnosa fisik : tekanan darah, berat badan, tinggi badan, hepar, lien, pembesaran kelenjar getah bening, massa abdomen (tempat dan ukuran). Anomali : hemihipertropi, genitalia external abnormal (hipospadia, criptosidism, duplikasi ureteral, ektopik ginjal), stigmata dari sindroma beckwith-wiedeman: aniridia, hamartroma.
- Data laboratorium : Darah lengkap, fungsi ginjal, fungsi hati, alkali phosphatase, LDH dan VMA.
Radiologi : foto thoraks (PA dan lateral), IVP, USG, CT Scan abdomen dengan kontras.
Pengobatan tumor
wilms terdiri dari operasi (pembedahan), kemoterapi dan radioterapi.
GEJALA KLINIK
Tumor dalam perut (tumor abdomen) merupakan gejala tumor Wilms yang paling sering(75-90%), yang sebagian besar diketahui pertama kali oleh orang tua atau keluarga penderita. Kadang-kadang ditemukan secara kebetulan oleh seorang dokter pada saat melakukan pemeriksaan fisik. Tumor Wilms dapat membesar sangat cepat, yang dalam beberapa keadaan disebabkan karena terjadinya perdarahan.
Hematuri (makroskopis) terdapat pada sekitar 25% kasus, akibat infiltrasi tumor ke dalam sistem kaliks. Hipertensi ditemukan pada sekitar 60% kasus, diduga karena penekanan tumor atau hematom pada pembuluh-pembuluh darah yang mensuplai darah ke ginjal, sehingga terjadi iskemi jaringan yang akan merangsang pelepasan renin, atau tumor sendiri mengeluarkan renin. Gejala lain berupa anemia, penurunan berat badan, infeksi saluran kencing, demam, malaise dan anoreksia. Pada beberapa penderita dapat ditemukan nyeri perut yang bersifat kolik, akibat adanya gumpalan darah dalam saluran kencing. Tumor Wilms tidak jarang dijumpai bersama kelainan kongenital lainnya, seperti aniridia, hemihipertrofi, anomali saluran kemih atau genitalia dan retardasi mental.
DIAGNOSIS
Diagnosis tumor Wilms berdasarkan atas :
- gejala klinik
- pemeriksaan radiologik (IVP dan USG), laboratorium LDH
- dipastikan dengan pemeriksaan histopatologik jaringan tumor
Dengan pemeriksaan IVP tampak distorsi sistem pielokalises (perubahan bentuk sistem pielokalises) dan sekaligus pemeriksaan ini berguna untuk mengetahui fungsi ginjal. USG merupakan pemeriksaan non invasif yang dapat membedakan tumor solid dengan tumor yang mengandung cairan.
Dengan pemeriksaan USG, tumor Wilms nampak sebagai tumor padat di daerah ginjal. Hasil pemeriksaan laboratorium yang penting yang menunjang untuk tumor Wilms adalah kadar lactic dehydrogenase (LDH) meninggi dan Vinyl mandelic acid (VMA) dalam batas normal.
Terapi
Modalitas pengobatan tumor Wilms terdiri dari, operasi (pembedahan), kemoterapi dan radioterapi. Pada tumor stadium I dan II dengan jenis sel favorable, dilakukan operasi dengan kombinasi kemoterapi dactinomycin dan vincristin tanpa pemberian radiasi abdomen. Tumor stadium III dengan jenis sel favorable diberikan pengobatan pembedahan dengan kombinasi daktinomisin, vinkristin dan doksorubisin disertai radiasi
abdomen. Untuk tumor stadium IV dengan jenis sel favorable, diberikan kombinasi daktinomisin, vinkristin dan doksorubisin. Penderita ini mendapat pula radiasi abdomen dan paru bila sudah ada penyebaran ke dalam jaringan paru.
Pada kasus stadium II sampai IV dengan jenis sel anaplastik (unfavorable) diberikan pengobatan pembedahan dengan kombinasi daktinomisin, vinkristin dan doksorubisin ditambah siklofospamid. Pada penderita ini menerima pula radiasi abdomen dan paru.
Prognosis
Beberapa faktor menentukan prognosis, yaitu ukuran tumor, gambaran histopatologik, umur penderita dan stadium atau tingkat penyebaran tumor. Mereka yang mempunyai prognosis yang baik adalah penderita yang mempunyai ukuran tumor masih kecil, tingkat diferensiasi sel tinggi secara histopatologik, stadium masih dini atau belum ada metastasis dan umur penderita di bawah dua tahun.
File: Dewasa Wilms’ tumor 1
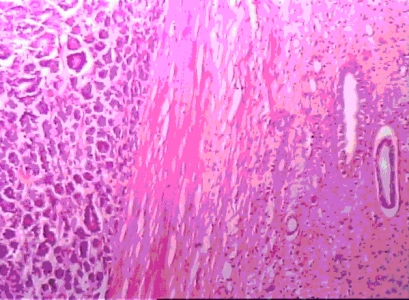
File: Dewasa Wilms' tumor 1
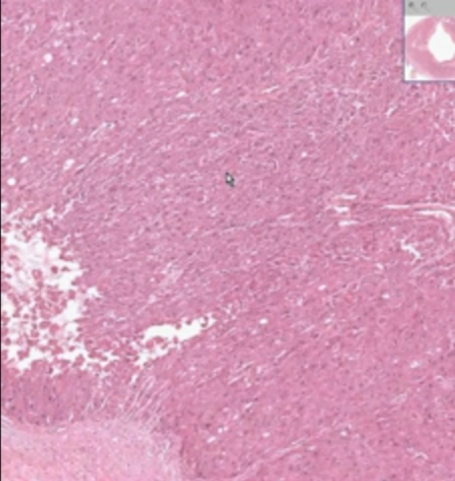
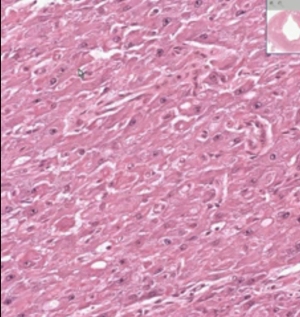
Triphasic menunjukkan pola tubules, solid lembar dari sel, dan stromal perbedaan dalam patologi contoh dewasa Wilms’ tumor.
Dewasa Wilms’ tumor 2
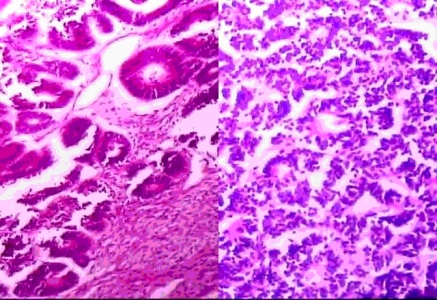
Dewasa Wilms' tumor 2
berbentuk tabung menyerupai pola pseudo-rosettes di tempat.
NONSTEROIDAL ANTIINFLAMMATORY DRUGS (NSAID)
nonsteroidal antiinflammatory drugs (NSAID) adalah sebagai penghambat sintesis prostaglandin, sedangkan kerja utama obat antiradang glukokortikoid menghambat pembebasan asam arakidonat. Selain dari kerja utama masih ada berbagai kerja lain pada NSAID dan obat antiradang glukokortikoid.
Mekanisme kerja
Asam arakidonat merupakan konstituen diet pada manusia, sebagai salah satu senyawa yang kehadirannya bersama diet asarn linoleat. Asam arakidonat sendiri oleh mernbran sel akan diesterifikasikan menjadi bentuk fosfolipid dan lainnya berupa kompleks lipid. Dalam keadaan bebas tetapi dengan konsentrasi yang sangat kecil asam ini berada di dalam sel. Pada biosintesis eikosanoid, asarn arakidonat akan dibebaskan dari sel penyimpan lipid oleh asil hidrolase. Besar kecilnya pembebasan tergantung dari kebutuhan enzim pensintesis eikosanoid. Kebutuhan ini ditentukan dari seberapa besar respons yang diberikan terhadap stimuli penyebab radang (Campbell, 1991).
Asam asetilsalisilat (aspirin) sebagai prototip nonsteroidal anti-inflammatory drugs (NSAID) merupakan analgetika nonsteroid, non-narkotik (Reynolds, 1982). Kerja utama asam asetilsaIisilat dan kebanyakan obat antiradang nonsteroid lainnya sebagai penghambat enzim siklooksigenase yang mengakibatkan penghambatan sintesis senyawa endoperoksida siklik PGG2 dan PGH2. Kedua senyawa ini merupakan prazat semua senyawa prostaglandin, dengan demikian sintesis rostaglandin akan terhenti (Mutschler, 1991; Campbell, 1991)
Asam asetilsalisilat (salisilat) tidak menghambat metabolisme asam arakidonat melalui alur lipoksigenase. Penghambatan enzim siklooksigenase kemungkinan akan menambah pembentukan leukotrien pada alur lipoksigenase. Kemungkinan ini dapat terjadi disebabkan bertambahnya sejumlah asam arakidonat dari yang seharusnya dibutuhkan enzim lipoksigenase (Mutschler, 1991; Campbell, 1991). Selain sebagai penghambat sintesis prostaglandin dari berbagai model eksperimen yang telah dicoba kepada manusia untuk tujuan terapeutik, NSAID ternyata menunjukkan berbagai kerja lain sebagai antiradang (Melmon dan Morreli, 1978).
Selain sebagai penghambat sintesis prostaglandin, beberapa contoh kerja lain NSAID adalah sebagai berikut. Fenilbutason (reumatoid artritis, pirai akut, sinovitis, ankilosing spondilitis dan osteoartritis), mirip asam asetilsalisilat yaitu uncouple oksidatif fosforilasi, interaksi dengan protein selular, menghambat pembebasan histamin, menghambat sintesis mukopolisakarida, menstabilkan membran lisosomal dan mengurangi respons terhadap enzim lisosomal (lnsel, 1991; Melmon dan Morreli, 1978). Indometasin (reumatoid dan beberapa tipe artritis termasuk pirai akut), menghambat motilitas leukosit polimorfonuklir, uncouple oksidatif fosforilasi dan menghambat sintesis mukopolisakarida (lnsel, 1991; Melmon clan Morreli, 1978). Turunan asam propionat (reumatoid artritis, osteoartritis dan ankilosing spondilitis), beberapa diantaranya dapat menghambat migrasi dan fungsi leukosit, khususnya naproksen sangat potensial. Ketoprofen dapat menstabilkan membran lisosomal dan aksi antagonis terhadap bradikinin (lnsel, 1991). Piroksikam (reumatoid artritis, osteoartritis), menghambat aktiviasi neutrofil (lnsel, 1991). Diklofenak (rheumatoid artritis, osteoartritis dan ankilosing spondilitis), mengurangi konsentrasi intraselular asam arakidonat bebas pada leukosit (lnsel, 1991).
NSAID yang khusus bekerja sebagai obat pirai, bukan sebagai penghambat sintesis prostaglandin. Kolkisin misalnya terutama diduga bekerja sebagai penghambat fungsi mikrotubule. Kerja lain adalah berinterferensi dengan aktivitas kalikrein, mencegah pembebasan histarnin in vitro dan menghambat respirasi selular dan motilitas leukosit polimorfonuklir (Melmon dan Morreli, 1978).